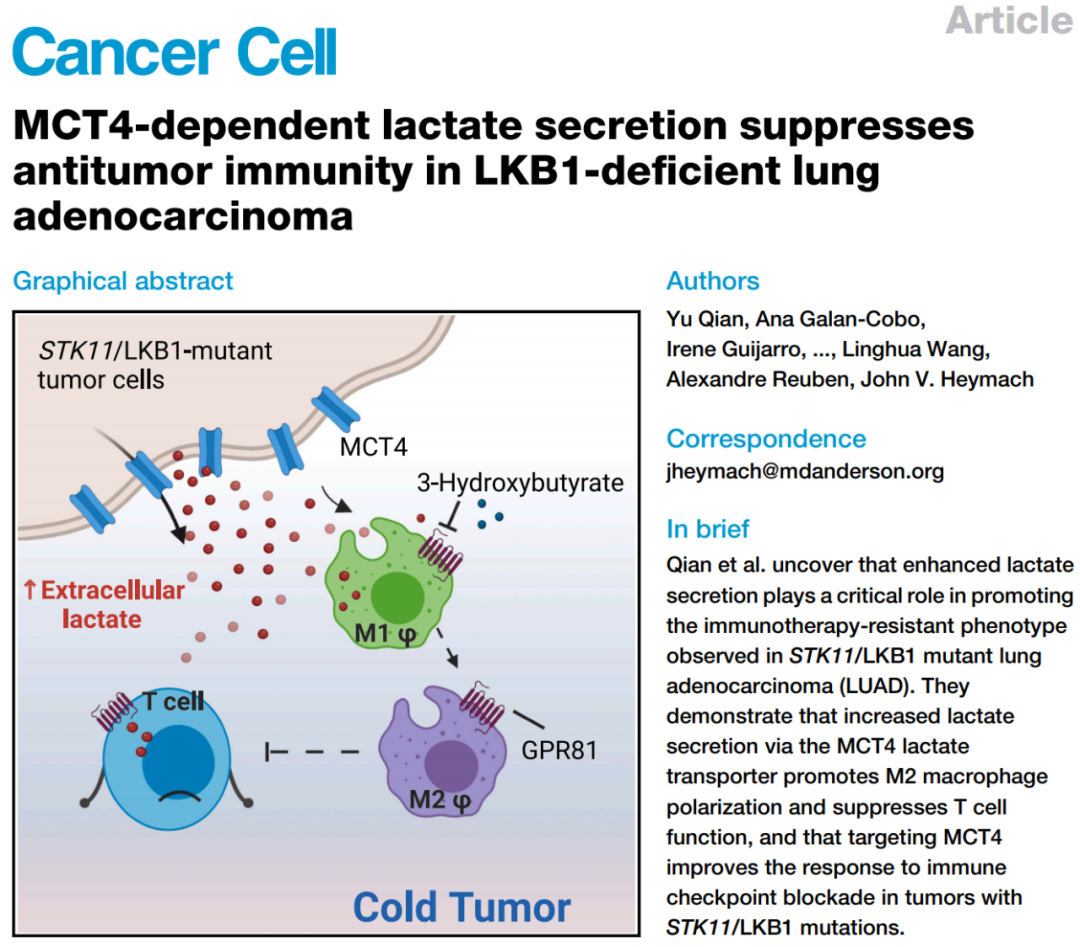
STK11(serine/threonine kinase 11)是一个重要的抑癌基因,其突变已被广泛证实与多种肿瘤类型的发生和发展相关。在肺癌中,STK11突变常常伴随着恶性程度的加剧和预后的恶化。最近的研究发现,在STK11突变型肺癌组织中,乳酸的水平显著升高。乳酸主要由肿瘤细胞通过糖酵解产生,其积累导致肿瘤微环境的酸化,这对抗肿瘤免疫应答产生了重要影响。
乳酸在肿瘤微环境中的积累可能通过多个机制抑制抗肿瘤免疫应答。首先,高水平的乳酸会降低免疫细胞的活性和功能。乳酸可以抑制细胞毒性效应,减少CD8+ T细胞和自然杀伤细胞(NK细胞)的杀伤能力,使得肿瘤细胞逃避免疫监视。其次,乳酸可以影响免疫细胞的迁移和侵袭能力,减少它们在肿瘤组织中的浸润和活动。此外,乳酸还改变了免疫细胞的代谢状态,导致细胞能量不足和功能受损。
乳酸的抑制作用还涉及免疫细胞亚群的选择性影响。研究表明,乳酸对不同类型的免疫细胞亚群有不同的影响。一方面,乳酸会选择性地抑制CD8+ T细胞和NK细胞的功能,破坏它们对肿瘤细胞的杀伤能力。另一方面,乳酸对树突状细胞等抗原呈递细胞的功能可能产生相反的影响,潜在地增加免疫抗原的呈递和激活效果。这种选择性影响对于免疫治疗的响应和效果具有重要意义。
乳酸的抑制作用还可能对免疫检查点抑制剂治疗产生影响。免疫检查点抑制剂(例如PD-1/PD-L1抗体)通过解除T细胞的抑制信号,激活免疫系统来对抗肿瘤。然而,乳酸的积累可能干扰T细胞的功能,降低它们对免疫检查点抑制剂的响应。此外,乳酸还与PD-L1表达水平和T细胞功能状态密切相关,进一步调节了免疫检查点抑制剂治疗的疗效。
针对STK11突变型肺癌中乳酸抑制抗肿瘤免疫应答的干预策略包括多个方面。一种策略是靶向乳酸代谢途径,抑制乳酸的产生和积累。这可以通过针对糖酵解途径的药物,如乳酸脱氢酶抑制剂或糖酵解抑制剂来实现。另一种策略是调节免疫细胞的功能和活性,增强它们对肿瘤细胞的杀伤能力。这可以通过免疫增强剂、免疫调节剂或细胞治疗等手段来实现。
总之,乳酸在STK11突变型肺癌中的抑制作用对抗肿瘤免疫应答具有重要意义。深入研究乳酸的作用机制,寻找有效的干预策略,对于提高STK11突变型肺癌患者的免疫应答,改善其预后具有重要意义。进一步的研究将有助于开发新的治疗策略,并为患者提供更有效的治疗选择。


