
阿尔茨海默病是一种常见的神经退行性疾病,严重影响患者的生活质量。尽管已经进行了大量的研究,但其病因和发病机制仍然不明确。最近,人类干细胞技术的进步使得研究人员能够在体外重建人类大脑发育的模型,为我们理解阿尔茨海默病的起源提供了新的机会。
人类大脑发育的干细胞模型: 该研究利用人类诱导多能干细胞(induced pluripotent stem cells, iPSCs)将其分化为神经前体细胞和神经元。通过模拟胚胎发育过程,研究人员成功地重建了人类大脑的神经系统,包括皮层、海马和杏仁核等关键结构。然后,他们引入了携带阿尔茨海默病相关基因突变的干细胞,以研究这些基因突变对大脑发育和阿尔茨海默病发病机制的影响。
阿尔茨海默病的胚胎起源: 研究结果表明,携带阿尔茨海默病相关基因突变的干细胞在人类大脑发育的早期阶段就表现出异常。这些细胞显示出异常的神经突触形成和连接,以及异常的细胞凋亡和炎症反应。此外,研究还发现,这些基因突变会导致β-淀粉样蛋白的异常积聚和Tau蛋白的磷酸化,这是阿尔茨海默病的典型特征。
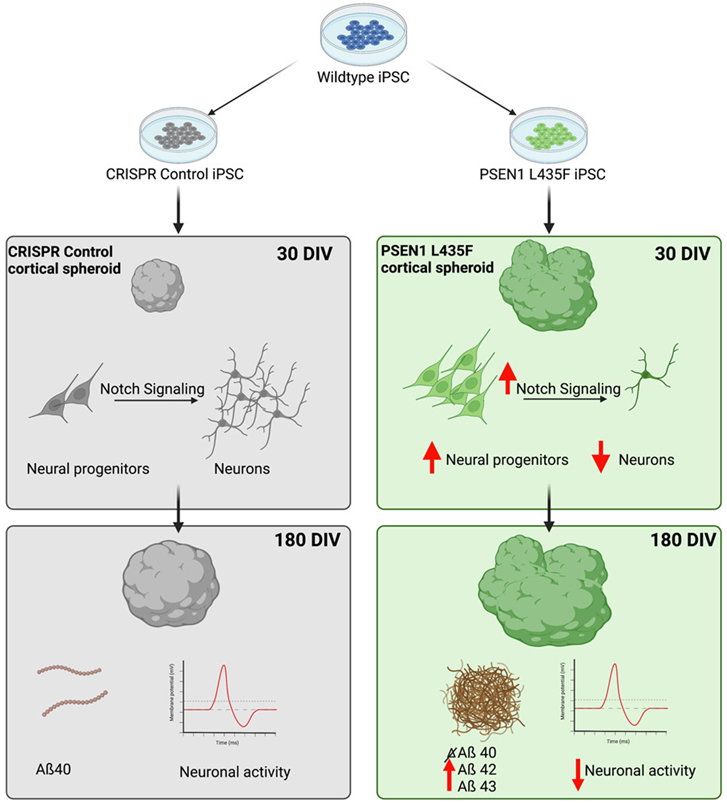
意义和展望: 这一研究的发现揭示了阿尔茨海默病的胚胎起源,为我们深入了解该疾病的发病机制和早期干预提供了重要线索。通过人类大脑发育的干细胞模型,我们可以更好地模拟阿尔茨海默病的病程,并研究潜在的治疗策略。此外,这一研究也为未来的药物开发提供了一个有效的平台,通过针对胚胎起源阶段的异常进行干预,可能有助于延缓或逆转阿尔茨海默病的进展。
结论: Cell子刊报道的研究利用人类大脑发育的干细胞模型揭示了阿尔茨海默病的胚胎起源。这一突破性研究为我们深入了解阿尔茨海默病的发病机制和早期干预提供了新的视角和机会。未来的研究将进一步深入探索这一模型,在药物开发和治疗策略上取得更大突破,为缓解阿尔茨海默病的全球负担做出更大贡献。


